Polyarthrite rhumatoïde
La polyarthrite rhumatoïde est la cause la plus fréquente des polyarthrites chroniques.
Recherche sur Google Images :
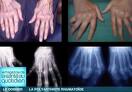
Source image : bonjour-docteur.com Cette image est un résultat de recherche de Google Image. Elle est peut-être réduite par rapport à l'originale et/ou protégée par des droits d'auteur. |
Définitions :
- maladie caractérisée par une inflammation articulaire chronique évoluant par poussées, d'étiologie inconnue, responsable de déformations... (source : protheses)
- Les premiers symptomes de la maladie sont le plus souvent des douleurs articulaires vives dans les poignets, les mains et les chevilles. Les articulations enflent, se raidissent et se déforment. Les causes de cette maladie sont nombreuses : choc psychologique, génétique, environnement.... (source : medicalreflex)
La polyarthrite rhumatoïde (PR) est la cause la plus fréquente des polyarthrites chroniques.
Elle est caractérisée par une atteinte articulaire fréquemment bilatérale et symétrique, évoluant par poussées vers la déformation et la destruction des articulations atteintes.
Le diagnostic peut en être malaisé au début de son évolution, à cause de l'absence de signe clinique spécifique, du caractère inconstant des signes biologiques, et du retard d'apparition des érosions articulaires radiologiques.
Synonymes
- polyarthrite chronique évolutive (PCE) (F. Costes et J. Forestier, 1929), polyarthrite rhumatismale, arthrite rhumatoïde, arthrodynie (Cullen), goutte asthénique primitive (Landré-Beauvais), polyarthrite chronique déformante ou p. c. inflammatoire ou p. c. rhumatismale (De sèze et Ryckewært) ou p. c. symétrique progressive (Bezançon et M. P. Weil), rhumatisme chronique déformant (Teissier et Roque) ou rh. ch. progressif généralisé ou rh. ch. progressif infectieux (Weissenbach et Françon) ou rh. articulaire chronique progressif (Charcot, 1853)
- Anglais : rheumatoid arthritis
Épidémiologie
La polyarthrite rhumatoïde est le plus habituel des rhumatismes inflammatoires de l'adulte.
On évalue sa prévalence entre 0, 3 et 0, 8 % selon les pays. En France, elle est localisée à 0, 4 %[1].
Il existe une nette prédominance féminine avec un sex-ratio de 3/1, mais cette différence semble s'atténuer avec l'âge.
Le pic de fréquence se situe autour de la quarantaine, cependant la maladie peut débuter à tout âge y compris chez l'enfant (cf. arthrites juvéniles idiopathiques).
Il existe certains facteurs de risque environnementaux, dont le tabagisme, le surpoids[2], l'exposition à la poussière de silice[3].
Causes
La polyarthrite rhumatoïde est une maladie auto-immune d'origine inconnue.
Elle met en jeu des facteurs hormonaux, environnementaux (infections…), sur terrain génétique prédisposé, la part de ce dernier dépasse probablement les 50%[4].
Les arguments pour une prédisposition génétique sont l'agrégation familiale de cas de polyarthrite rhumatoïde et la présence chez les sujets atteints des allèles HLA DR1 et DR4 dans 60 % des cas. La présence d'une mutation sur le gène PTPN22 qui code une tyrosine phosphatase double aussi le risque de développer la maladie qui est quelquefois plus grave[5]. Une mutation du gène TRAF1–C5 localisé sur le chromosome 9 est aussi corrélé avec une forme plus grave de la polyarthrite rhumatoïde (avec présence d'anticorps anti-CCP : cyclic citrullinated peptide) [6].
Les mécanismes immunologiques effecteurs sont multiples :
- stimulation des lymphocytes T CD4+,
- stimulation des lymphocytes B et différentiation en plasmocytes, responsables entre autres de sécrétion de facteurs rhumatoïdes et autres auto-anticorps
- sécrétion de cytokines pro-inflammatoires intra-articulaire, essentiellement le TNFalpha, à l'origine des synovites et des érosions articulaires.
Signes cliniques au début
La maladie commence le plus souvent par une polyarthrite, c'est-à-dire l'inflammation de quatre articulations ou plus, caractérisée par des douleurs d'horaire inflammatoire (réveils nocturnes, dérouillage matinal de durée supérieure à 30 minutes), une raideur articulaire et un gonflement nommé synovite.
Il existe peu de signes spécifiques pour différencier la polyarthrite rhumatoïde des autres causes de polyarthrite (cf. diagnostics différentiels). Cependant, certaines caractéristiques cliniques sont évocatrices :
- L'évolution progressive et insidieuse : subaiguë, c'est-à-dire évoluant depuis plus de 2 semaines, ou en particulier chronique évoluant depuis plus de 3 mois ;
- Le siège des synovites aux petites articulations : poignets et chevilles et en particulier mains et pieds au niveau des interphalangiennes proximales (ou IPP, entre 1re et 2e phalanges) et articulations métacarpo-phalangiennes (ou MCP, entre le métacarpien et la 1re phalange). L'ensemble des articulations peuvent cependant être atteintes en cours d'évolution : genoux, coudes, épaules, hanches, articulations temporo-mandibulaires… Par contre, les interphalangiennes distales (entre les 2e et 3e phalanges) et les sacro-iliaques sont toujours respectées. Le rachis est aussi épargné, à l'exception du rachis cervical.
- La topographie généralement bilatérale et symétrique.
- L'intensité des signes inflammatoires locaux : tuméfaction chaude et douloureuse donnant l'aspect classique de "doigts en fuseaux" ;
- La cœxistence de ténosynovites (inflammation des tendons musculaires) ;
- L'association envisageable à des nodosités cutanées nommées nodules rhumatoïdes. Situés sur la face d'extension des coudes des doigts ou sur le tendon d'Achille, ils sont particulièrement spécifiques de la polyarthrite rhumatoîde mais inconstants et tardifs.
Examens biologiques
Il existe le plus souvent un syndrome inflammatoire quand la maladie est en poussée, se traduisant par une augmentation de la vitesse de sédimentation et de la protéine C réactive. Il peut s'accompagner d'une hyperleucocytose à prédominance de polynucléaires neutrophiles et d'une anémie inflammatoire non spécifiques.
Les examens immunologiques dans le sérum peuvent retrouver :
- un facteur rhumatoïde, détecté par les réactions de latex, Waaler-Rose, ou par des techniques plus modernes comme l'ELISA ou la néphélométrie. Le facteur rhumatoïde est une immunoglobuline (d'isotype M, G ou A) dirigée contre le fragment constant d'une autre immunoglobuline d'isotype G. Test sensible puisque présent dans 80% des polyarthrites rhumatoïdes, le dosage du facteur rhumatoïde présente l'inconvénient d'une faible spécificité (environ 50%) avec une fréquente positivité dans la plupart d'autres maladies. De plus, le test est souvent négatif en début d'évolution et ne se positive qu'au cours de la première année d'évolution.
- des anticorps anti-CCP (cyclic citrullinated peptide) : présents dans uniquement à peu près 60% des cas mais particulièrement spécifiques de la maladie (environ 95%) [7]. Il est d'ailleurs envisageable que les polyarthrites rhumatoïdes ne comportant pas ce type d'anticorps soient une forme différente de la maladie, le tabagisme, par exemple, influançant négativement les porteurs et restant sans effet chez les non-porteurs[8].
- rarement, des Anticorps antinucléaires à faible taux (30%).
La ponction articulaire retrouve plus de 1 000 leucocytes par millimètre cube, confirmant le caractère inflammatoire de l'épanchement. Elle n'a pas cependant pas d'intérêt pour le diagnostic sauf en cas de doute sur une polyarthrite de cause infectieuse (recherche de germe dans le liquide articulaire) ou microcristalline (recherche de cristaux d'urate de sodium dans la goutte, de pyrophosphate de calcium dans la chondrocalcinose).
Examens radiologiques
Le bilan radiographique d'origine minimal comporte des clichés des mains/poignets et des avant-pieds de face et de trois-quarts, des clichés de la totalité des articulations douloureuses et une radiographie pulmonaire.
Au cours de l'évolution, la surveillance des destructions doit comporter un bilan radiographique l'ensemble des six mois pendant les deux premières années, puis l'ensemble des ans à l'ensemble des deux ans. Un cliché dynamique du rachis cervical en flexion forcée doit être réalisé régulièrement pour dépister les complications cervicales de la maladie.
Les signes radiologiques :
- Ils sont discrets au début : déminéralisations osseuses périarticulaires, se traduisant par une hypertransparence osseuse autour des articulations, signe non spécifique présent dans la totalité des rhumatismes inflammatoires. Il existe un épaississement des parties molles périarticulaires.
- Plus tard apparaîtront les destructions articulaires caractéristiques de la polyarthrite rhumatoïde : pincement de l'interligne articulaire, microgéodes (sortes de "trous" dans l'os sous-chondral) et érosions osseuses. L'érosion de la tête du 5e métatarsien, visible sur une radiographie des avant-pieds, forme classiquement la destruction articulaire la plus précoce et est d'un grand intérêt diagnostique.
- L'aboutissement des lésions est la destruction articulaire complète correspondant aux déformations observées à l'examen au bout de plusieurs années d'évolution : subluxations des métacarpo-phalangiennes et des interphalangiennes, flessum des coudes et genoux, ankyloses surtout du carpe (=poignet) etc...
Évolution
Évolution articulaire
Le plus fréquemment, l'évolution, qui s'étale sur des dizaines d'années, se fait par poussées, entrecoupées de rémissions de rythme et de durée imprévisibles. Au cours des poussées, la majorité des articulations sont gonflées et douloureuses, associées à des signes généraux (fièvre modérée ou fébrilcule, asthénie) et souvent d'un syndrome inflammatoire biologique. Le suivi de l'activité de la maladie peut se faire avec différents scores. Le plus utilisé en pratique clinique est le «DAS 28», calculé à partir de quatre paramètres : l'indice articulaire (nombre d'articulations douloureuses - sauf pieds chevilles et hanches non comptabilisées), l'indice synovial (nombre d'articulations gonflées - sauf pieds chevilles et hanches), activité de la maladie évaluée sur une échelle de 0 à 100 par le patient, et vitesse de sédimentation.
Après plusieurs années d'évolution apparaissent les déformations caractéristiques, secondaires à la destruction articulaire ainsi qu'à l'atteinte tendineuse :
- aux poignets : subluxation antérieure de la main, subluxation postérieure de la tête cubitale «en touche de piano» pouvant conduire à la rupture du tendon extenseur du 5e doigt.
- aux mains : déformations des doigts en maillet (flexion de l'interphalangienne distale), en col de cygne (flexion de l'interphalangienne distale et hyperextension de l'interphalangienne proximale), ou en boutonnière (hyperextension de l'interphalangienne distale et flexion de l'interphalangienne proximale) ; déformation du pouce en Z ; fréquent«coup de vent cubital» des doigts (déviation latérale des doigts) ; aspect des mains «en dos de chameau» (gonflement des rangées des métacarpo phalangiennes et carpiennes et atrophie des muscles interosseux)
- aux coudes et genoux : flessum irréductible ;
- aux pieds : orteils «en marteau» ou en griffe, coup de vent péronier (déviation latérale des orteils), hallux valgus (déviation interne du 1er orteil) et quintus varus (déviation interne du 5e orteil) aboutissant à un avant-pied triangulaire, affaissement de la voûte plantaire ;
- enraidissement des hanches et des épaules ;
- sur le rachis cervical : atteinte tardive, comportant surtout une envisageable subluxation atloïdo-axoidienne qui concerne les deux premières vertèbres et peut conduire à une compression de la mœlle épinière cervicale en l'absence de traitement.
- ruptures tendineuses compliquant l'évolution des ténosynovites.
Dans les polyarthrites particulièrement évoluées, les poussées inflammatoires ont tendance à devenir moins habituelles. On assiste alors à l'extinction progressive de la maladie. À ce stade, les douleurs sont plus souvent d'horaire mécanique (prédominance le soir ainsi qu'aux mouvements, absence de dérouillage articulaire matinal) liées aux destructions articulaires.
La polyarthrite rhumatoïde est une affection d'évolution et de gravité particulièrement hétérogènes. Le retentissement fonctionnel, socioprofessionnel, psychologique peut être énorme. Schématiquement on considère que 30% sont d'évolution assez bénigne, 50% intermédiaires et 20% sévères. La définition de la sévérité n'est cependant pas consensuelle aujourd'hui.
Actuellement, on rattache la gravité d'une polyarthrite rhumatoïde à l'altération de la qualité de vie qu'elle entraîne, évaluée par le score HAQ (Health Assessment Questionnaire) ainsi qu'à l'importance des destructions articulaires.
Évolution extra-articulaire
D'autres atteintes portant sur des organes extra-articulaires sont envisageables : poumons, cœur, dispositif nerveux périphérique, "syndrome sec" avec l'œil sec et bouche sèche (syndrome de Gougerot-Sjögren).
Traitement
La stratégie thérapeutique comporte plusieurs volets
Traitement symptomatique
Il permet le soulagement des symptômes. Il peut comporter le repos simple lors des poussées, les traitements antalgiques classiques, les anti-inflammatoires non stéroïdiens, les corticostéroïdes à faible dose, inférieure à 10 mg/jour pour en limiter les effets secondaires. Dans les poussées particulièrement inflammatoires polysynoviales, un ou plusieurs bolus peuvent être réalisées pour soulager rapidement le patient en attendant l'efficacité d'un nouveau traitement de fond.
Traitements de fond
Ils sont aussi nommés " DMARD" (disease modifying anti-rheumatic drugs) visant à contrôler les manifestations inflammatoires cliniques de la maladie, ainsi qu'à freiner son évolution destructrice. Leur efficacité est généralement retardée (un à trois mois), suspensive (reprise d'activité à l'arrêt), et malheureusement inconstante, et épuisable obligeant à changer de molécule. Ils doivent par conséquent être constamment adaptés à l'activité inflammatoire ainsi qu'à la sévérité de la maladie.
Principales molécules
Quasiment abandonnés en raison d'une tolérance médiocre, ce sont les sels d'or et la D-pénicillamine.
Utilisé dans les polyarthrites peu actives et non érosives ou dans les polyarthrites inclassées, ce sont les antipaludéens de synthèse comme l'hydroxychloroquine (Plaquénil). Il possède une efficacité clinique mais ne prévient pas les destructions.
Le méthotrexate est utilisé en première intention à la dose de 10 à 20 mg/ semaine, par voie orale, sous-cutanée ou intra-musculaire. D'autres molécules sont aussi employées : léflunomide (Arava) ; sulfasalazine, (Salazopyrine). L'association de ces molécules (en particulier, salazopyrine + méthotrexate +/- hydroxyplaquenil) pourrait en perfectionner l'efficacité ; cependant, cette idée reste discutée.
Dans les formes sévères, certains immunosuppresseurs comme l'azathioprine (Imurel), la ciclosporine (Neoral, Sandimmum) peuvent être employés.
Réservées aux formes sévères d'emblée, ou en cas d'échec ou d'échappement aux traitements qui ont précédé sont les les biothérapies :
- les anti-TNF alpha : infliximab (Remicade) en perfusions de 3 à 5 mg/kg l'ensemble des 8 semaines, Etanercept (Enbrel), adalimumab (Humira). Leur efficacité clinique et radiologique est fréquemment spectaculaire, au prix d'effets secondaires de gravité variable, essentiellement infectieux (en particulier tuberculose mais également autres infections bactériennes et virus). L'initiation du traitement, de prescription hospitalière, comporte une recherche systématique de foyer infectieux et surtout d'une tuberculose latente. Ces molécules doivent toujours être associées à un autre traitement de fond (méthotrexate, léflunomide…) pour prévenir la naissance d'anticorps anti-antiTNFalpha, qui faciliteraient les résistances et les allergies au traitement.
- Un inhibiteur du CTLA4 : l'abatacept commercialisé sous le nom d'Orancia® est accepté en France, dans la prise en charge des polyarthrites réfractaires aux anti TNF, il s'administre sous forme de perfusions mensuelles à la dose de 8 mg/ kg en une vingtaine de minutes.
- les antagonistes du récepteur de l'interleukine-1 : anakinra (Kineret), peu utilisés en raison d'une efficacité médiocre.
- les anti-CD20 : rituximab (Mabthera), après échec des anti-TNF alpha sont aussi disponibles, Ils sont utilisés en association avec des perfusions de corticoides, deux perfusions à 15 jours d'intervalles, et ont un effet de déplétion des lymphocytes B sur au moins six mois.
- en cours d'évaluation : un nouvel anti-TNF alpha, le golimumab ; un anti-Il6 : le MRA ; d'autres anti CD 20 Ocrelizumab, et des inhibiteurs des MAP kinases.
Outre les molécules, les stratégies d'utilisations des traitements semblent aussi particulièrement importantes pour obtenir une rémission, plusieurs études comme TICORA, Fin RaCo, et BEST surtout suggèrent que l'utilisation précoces d'une combinaison de traitement de fond à bonne dose et tôt dans l'histoire de la maladie donnait plus de rémission, et permet plus fréquemment l'arrêt des anti TNF, que dans les suites d'une initiation tardive. Qui plus est la mesure du DAS l'ensemble des trois mois avec un Seuil à 2, 4 forme un élément décisionnel important dans l'obtention d'une rémission.
Traitements locaux
Les infiltrations intra-articulaires de dérivés corticoïdes sont à visée symptomatique, dans le cas d'une ou de quelques articulations gonflées malgré une maladie peu active d'autre part.
La synoviorthèse isotopique (injection intra-articulaire d'isotopes radioactifs) ou chimique (injection d'acide osmique), consistent en la destruction de la synoviale d'une articulation restant inflammatoire malgré les infiltrations de corticoïdes.
La chirurgie a certaines indications : synovectomie d'une petite articulation inflammatoire malgré les mesures précédentes, ténosynovectomie ; au stade tardif de destruction articulaire : correction d'une déformation invalidante ou douloureuse (arthrodèse du poignet ou de l'arrière pied…), ou arthroplastie qui concerne essentiellement les grosses articulations : hanches, genoux, épaules, plus rarement poignets et métacarpophalangiennes ; réparation d'une rupture tendineuse.
Rééducation
La physiothérapie sert à diminuer la douleur et l'inflammation lors des poussées inflammatoires.
La kinésithérapie, les règles d'hygiène de vie, l'éducation gestuelle et les exercices posturaux sont d'un appoint non négligeable.
L'ergothérapie consiste en la confection d'attelles de repos (portées au cours de la nuit) et orthèses qui s'opposent aux attitudes vicieuses ainsi qu'aux déformations articulaires. Elle permet l'aide à la réadaptation du patient dans son environnement habituel.
Traitement non conventionnel
Des extraits d'une plante médicinale, Tripterygium wilfordii, pourraient avoir, occasionnellemen, une efficacité au moins équivalente à celle de la sulfasalazine [9].
Autres mesures
L'information concernant la maladie, individuellement et au sein de groupes de patients, reste indispensable. Elle peut être associée à une orientation vers des associations de malades.
En France, les soins sont pris en charge à 100% au titre de l'ALD 30.
Diagnostic différentiel
| CLASSEMENT | PENSER D'ABORD À | PUIS À |
|---|---|---|
| Polyarthrites bactériennes | Septicémie Endocardite Gonocoque |
Brucellose Maladie de Lyme Tuberculose |
| Polyarthrites virales | Hépatite B et C Parvovirus B19 |
Oreillons, rubéole mononucléose infectieuse, cytomégalovirus (CMV) VIH |
| Polyarthrites "post-infectieuses" | Arthrites réactionnelles (post Chlamydiæ, Shigella, Yersinia, Campylobacter…) | RAA (rhumatisme articulaire aigu) Rhumatisme post-streptococcique |
| Polyarthrites "métaboliques" | goutte Chondrocalcinose |
|
| Rhumatismes inflammatoires | ||
| Maladies auto-immunes | Lupus systémique] Syndrome de Gougerot-Sjögren |
Autres connectivites Vascularites Sarcoïdose |
Voir aussi
| Polyarthrite rhumatoïde | |
| CIM-10 : | M05-M06 |
|
{{{CIM10}}}. 0 {{{X. 0}}} |
|
| M05-M06.1 {{{X. 1}}} | |
| M05-M06.2 {{{X. 2}}} | |
| M05-M06.3 {{{X. 3}}} | |
| M05-M06.4 {{{X. 4}}} | |
| M05-M06.5 {{{X. 5}}} | |
| M05-M06.6 {{{X. 6}}} | |
| M05-M06.7 {{{X. 7}}} | |
| M05-M06.8 {{{X. 8}}} | |
| M05-M06.9 {{{X. 9}}} | |
Liens externes
- (fr) La polyarthrite rhumatoïde sur le site du COFER (collège français des enseignants en rhumatologie)
- (fr) Association Française des Polyarthritiques
- (fr) Association Nationale de Défense contre l'Arthrite Rhumatoïde
Notes et références
- ↑ Guillemin F, Saraux A, Guggenbuhl P, Roux CH, Fardellone P, Le Bihan E et als. Prevalence of rheumatoid arthritis in France : 2001, Ann Rheum Dis, 2005;64 :1427-30.
- ↑ Symmons DP, Bankhead CR, Harrison BJ et als. [Blood transfusion, smoking, and obesity as risk factors for the development of rheumatoid arthritis : results from a primary care-based incident case-control study in Norfolk, England], Arthritis Rheum, 1997;40 : 1955-1961
- ↑ Klockars M, Koskela RS, Jarvinen E, Kolari PJ, Rossi A, Silica exposure and rheumatoid arthritis : a follow up study of granite workers 1940—81, BMJ, 1987;294 :997-1000
- ↑ MacGregor AJ, Snieder H, Rigby AS et als. Characterizing the quantitative genetic contribution to rheumatoid arthritis using data from twins, Arthritis Rheum, 2000;43 :30-37
- ↑ Begovich AB, Carlton VE, Honigberg LA et als. A missense single-nucleotide polymorphism in a gene encoding a protein tyrosine phosphatase (PTPN22) is associated with rheumatoid arthritis, Am J Hum Genet, 2004;75 :330-337
- ↑ Plenge RM, Seielstad M, Padyukov L et Als. TRAF1–C5 as a Risk Locus for Rheumatoid Arthritis — A Genomewide Study, New Eng J Med, 2007;357 :1199-1209
- ↑ Nishimura K, Sugiyama D, Kogata Y et Als, Meta-analysis : Diagnostic accuracy of anti–cyclic citrullinated peptide antibody and rheumatoid factor for rheumatoid arthritis, Ann Int Med, 2007;146;797-808
- ↑ Linn-Rasker SP, van der Helm-van Mil AH, van Gaalen FA et als. Smoking is a risk factor for anti-CCP antibodies only in rheumatoid arthritis patients who carry HLA-DRB1 shared epitope alleles, Ann Rheum Dis, 2006;65 :366-371
- ↑ Goldbach-Mansky R, Wilson M, Fleischmann R, Comparison of Tripterygium wilfordii Hook F versus sulfasalazine in the treatment of rheumatoid arthritis, Ann Int Med, 2009;151 :229-240
Recherche sur Amazone (livres) : |
Voir la liste des contributeurs.
La version présentée ici à été extraite depuis cette source le 22/11/2009.
Ce texte est disponible sous les termes de la licence de documentation libre GNU (GFDL).
La liste des définitions proposées en tête de page est une sélection parmi les résultats obtenus à l'aide de la commande "define:" de Google.
Cette page fait partie du projet Wikibis.


 Accueil
Accueil Recherche
Recherche Début page
Début page Contact
Contact Imprimer
Imprimer Accessibilité
Accessibilité